Dyspnea 臨床教學文件
From Bench to Bedside — 每分鐘 12 次呼吸裡的秘密
A — BENCH呼吸控制的基礎科學
A1 為什麼要懂呼吸控制?
你每分鐘呼吸大約 12-16 次,幾乎不需要想。但是一旦呼吸出問題,病人進來說「我覺得喘」——你要能回答:是哪裡出了問題?
根據 Murray & Nadel's Textbook(Schwartzstein & Adams),呼吸系統可以想成三個角色[1]:
感測器(Sensors):像偵探,隨時監測身體的 CO₂、O₂、pH、和各種機械壓力。
控制中樞(Controller):像指揮官,收到偵探的報告後決定該怎麼呼吸。
效應器(Effectors):像士兵,就是你的呼吸肌——膈肌、肋間肌,接到命令就收縮。
這三個角色任何一個出問題,都會讓人覺得喘。而且——這是最關鍵的——不同的問題會讓病人產生不同「質感」的喘。Schwartzstein & Adams 把 dyspnea 歸納為四種產生方式[1]:
- 血液氣體異常 → 化學受體被激活:低氧、高 CO₂ 或酸中毒刺激化學受體 → 大腦命令「多呼吸!」→ 病人感覺「吸不夠空氣」
- 肺部感受器被直接刺激:肺裡的 C 纖維、irritant receptors 被炎症或水腫激活 → 產生「胸悶」或窒息感
- 機械負荷增加:氣道阻力變大(如 COPD)或肺變硬(如纖維化)→ 呼吸肌要更用力 → 病人感覺「好費力」
- 呼吸肌無力:肌肉本身沒力氣(如 Guillain-Barré、肌無力症)→ 大腦拼命下令但肌肉做不到 → 最令人痛苦的喘
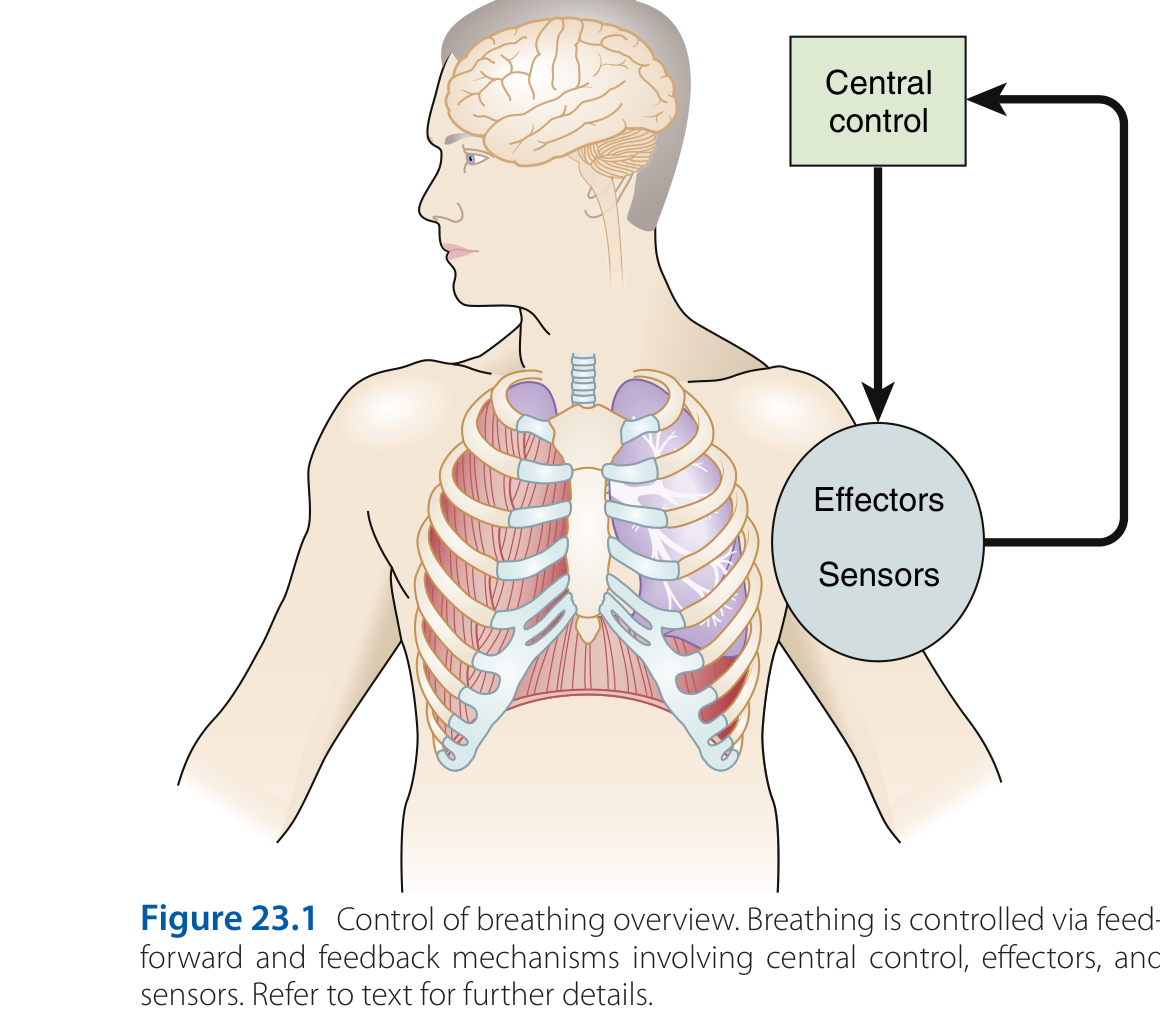
中文說明:呼吸就是一個自動控制迴路。「偵探」(感測器)回報 →「指揮官」(腦幹)下令 →「士兵」(呼吸肌)執行 → 結果再被偵探偵測。任何環節出錯就會喘。
A2 大腦怎麼控制呼吸
呼吸有一個很特別的地方:你可以故意憋氣、深呼吸或唱歌(隨意控制),但睡著或昏迷時呼吸照常(自動控制)。根據 Guyton & Hall Textbook of Medical Physiology[2],自動呼吸的節律是由腦幹的呼吸中樞產生的。
Guyton 描述呼吸中樞有三大部分[2]:
- 背側呼吸群(Dorsal Respiratory Group):主管吸氣。它像一個節拍器,每次放電就產生一次吸氣動作。放電訊號不是突然開關,而是像「爬坡」一樣逐漸增強(ramp signal),讓吸氣平滑地進行
- 腹側呼吸群(Ventral Respiratory Group):裡面有一個叫 pre-Bötzinger complex 的區域,被認為是呼吸節律的「中央發電廠」(central pattern generator)。平靜呼吸時它安靜工作;用力呼吸時它同時驅動吸氣和呼氣
- 呼吸調整中樞(Pneumotaxic Center):位於橋腦,功能是控制吸氣的「長度」。它的訊號越強,吸氣時間越短,呼吸頻率就越快
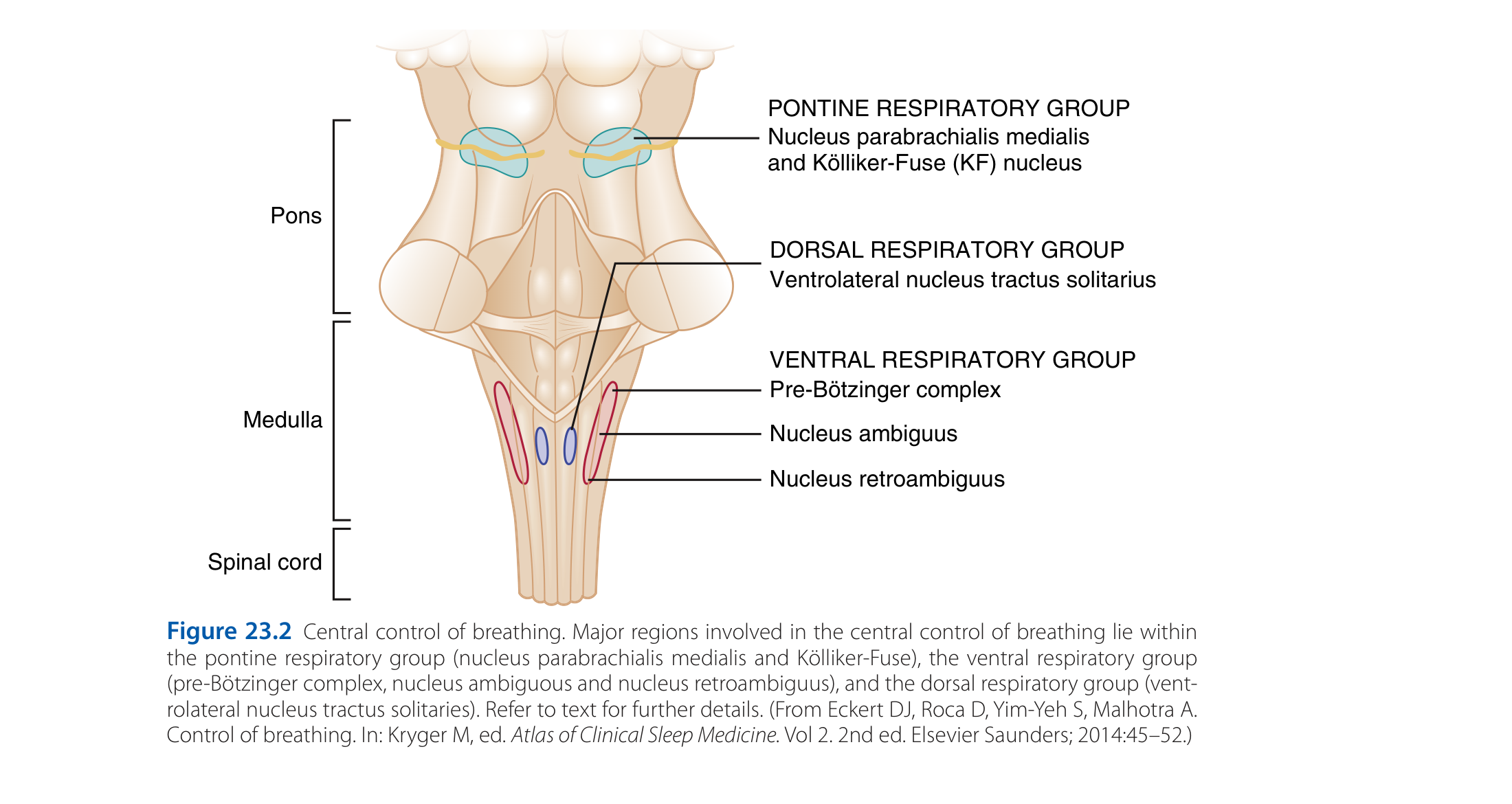
中文說明:腦幹的三大呼吸中樞各有分工。DRG 主管吸氣節拍;VRG(含 pre-Bötzinger complex)是節律發電廠;橋腦的 pneumotaxic center 控制每次吸氣的長短。三者協力讓你每分鐘自動呼吸 12-16 次。
另外,Guyton 提到一個重要的反射:Hering-Breuer 膨脹反射[2]。當肺膨脹到一定程度,肺裡的 stretch receptors(牽張受體)會通過迷走神經告訴腦幹「夠了,停止吸氣」。這是一個保護機制,防止肺被過度膨脹。
A3 身體怎麼知道該喘
腦幹要知道「現在該呼吸多少」,靠的是各種感測器的回報。Guyton 把最重要的一句話寫得很清楚[2]:
CO₂ 和 H⁺ 直接作用於延髓的化學敏感區(ventrolateral medulla 和 retrotrapezoid nucleus),大幅增強呼吸驅動。相反,O₂ 不直接影響腦幹——它只能通過周邊化學受體(頸動脈體和主動脈體)間接發揮作用。[2]
為什麼 CO₂ 比 O₂ 重要?Guyton 解釋[2]:血液中的 CO₂ 能穿過血腦屏障(blood-brain barrier),到達腦脊液後轉化為 H⁺,直接刺激化學敏感區。但 H⁺ 本身穿不過血腦屏障。所以 CO₂ 是「信差」——它帶著酸鹼的信息進入大腦。
Guyton 的經典圖表(Figure 42.3)清楚呈現了這個關係[2]:當 PCO₂ 從正常值(40 mmHg)升高到 60 mmHg,通氣量可以暴增到原來的 5-6 倍(紅色曲線的陡峭上升)。相較之下,pH 的變化對通氣量的影響小得多(藍色曲線較平緩)。
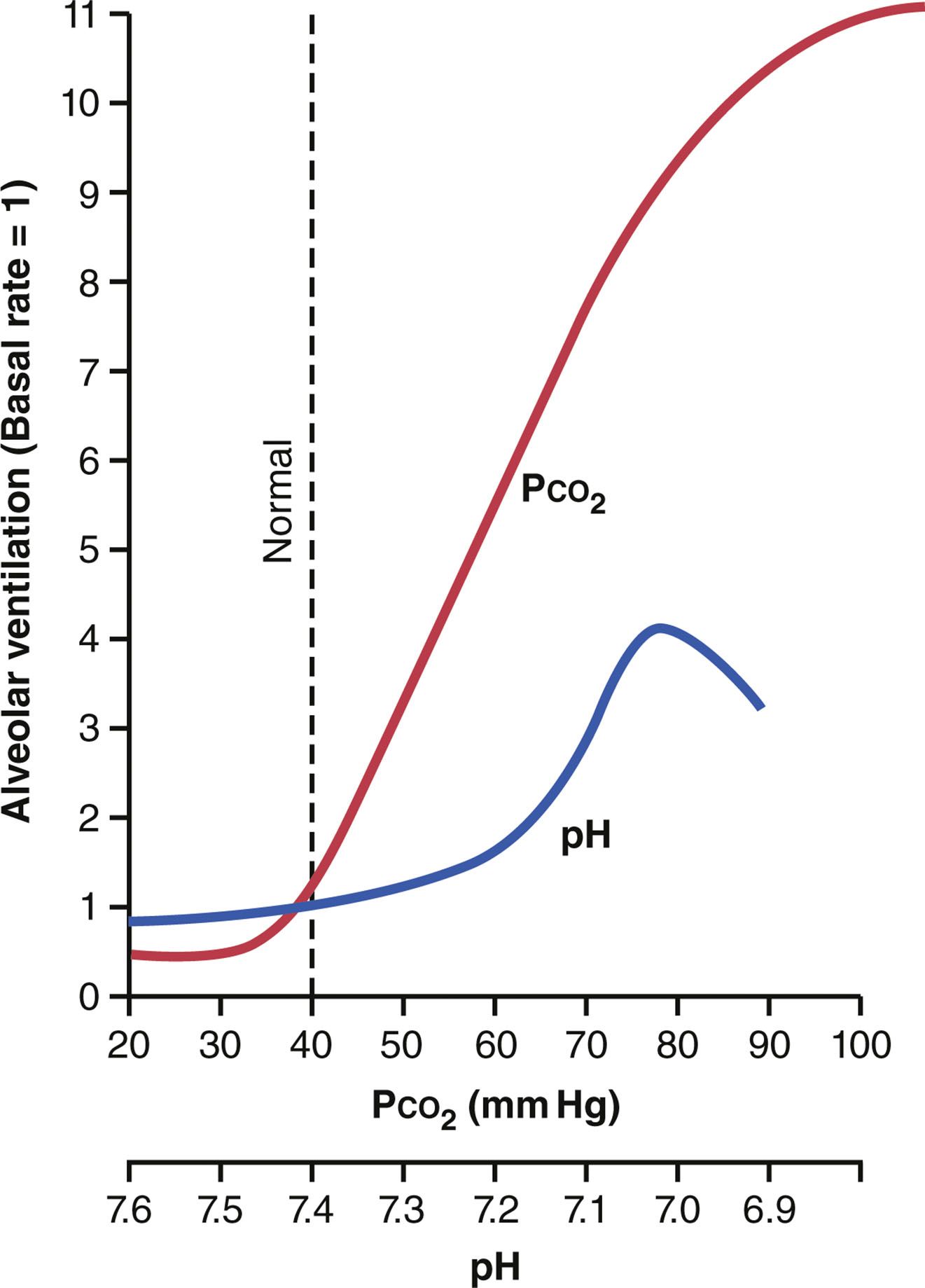
中文說明:這張圖是理解呼吸驅動的「黃金圖」。紅色曲線(PCO₂)在正常值(40 mmHg,虛線處)右邊急劇上升——表示 CO₂ 一升高,通氣量就暴增。藍色曲線(pH)相對平緩——表示 H⁺ 的效果弱得多。臨床意義:CO₂ 是呼吸系統最敏感的驅動器,PCO₂ 只要升高幾個 mmHg,通氣量就大幅增加。
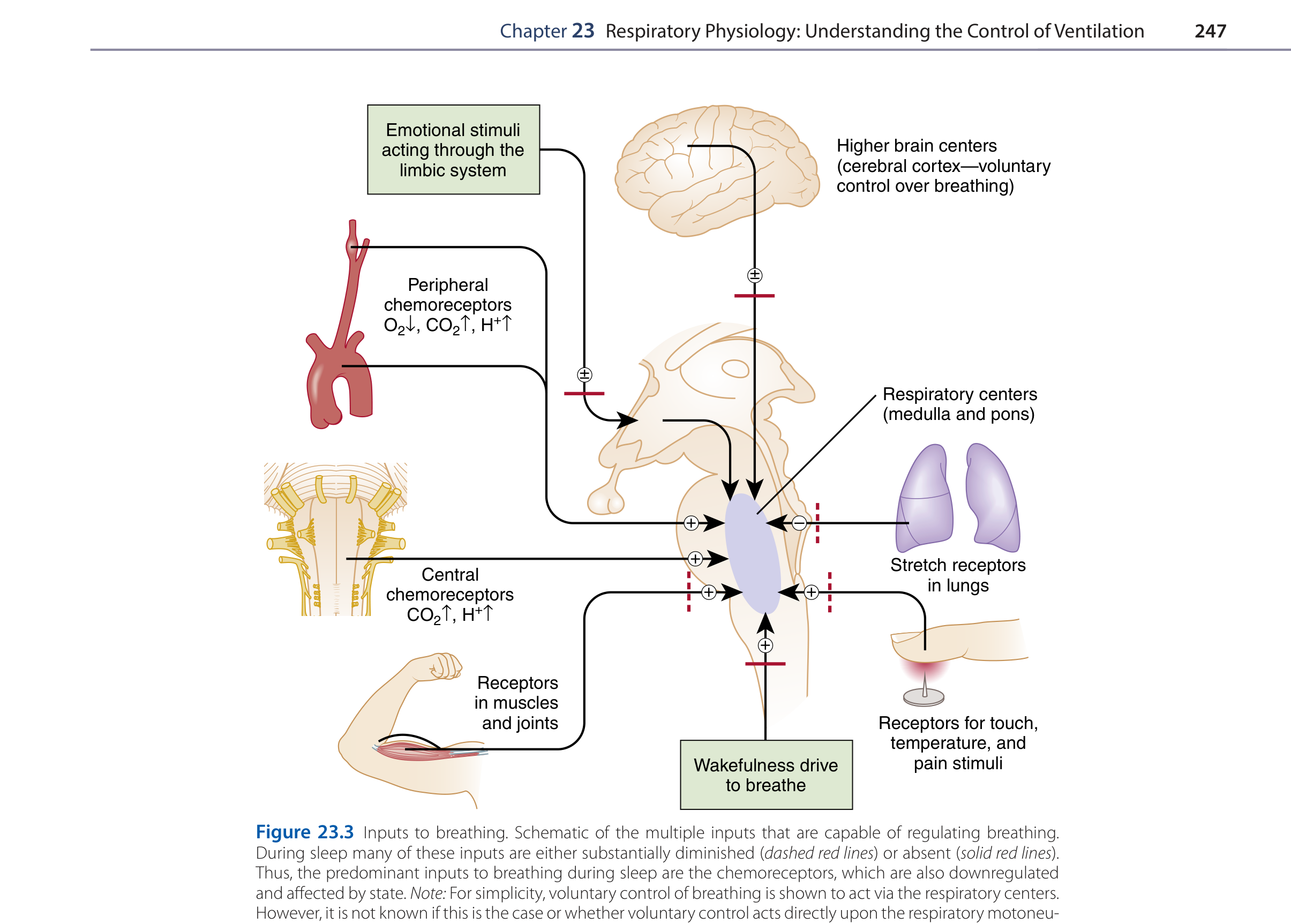
中文說明:呼吸受到很多種「偵探」的監測。最重要的是化學受體(監測 CO₂、O₂、pH)。另外還有肺的機械受體(stretch, irritant, C fibers)、胸壁受體、和肌肉的代謝受體。注意:睡眠時很多輸入會減弱甚至消失(紅色虛線和實線),只剩化學受體還在值班。這就是為什麼有些病人睡眠時呼吸會出問題。
周邊化學受體的補充[2]:頸動脈體(通過舌咽神經 CN IX 傳入)和主動脈體(通過迷走神經 CN X 傳入)主要感知低氧。但重點是——低氧要降到 PaO₂ < 60 mmHg 才會明顯刺激呼吸。所以在正常範圍內,O₂ 對呼吸驅動的貢獻很小。
除了化學受體,Murray & Nadel's Textbook[1] 列出了六種「非化學受體」的感測器,它們全都位於心肺系統或骨骼肌,經由不同路徑把訊息送回腦幹。以下逐一拆解:
① 肺 C 纖維(Pulmonary C fibers / Juxtacapillary receptors, J receptors)
受體類型:無髓鞘神經末梢(unmyelinated nerve endings),屬於迷走神經的 C 纖維傳入[1]。它們藏在肺泡壁和肺微血管旁邊(所以叫 juxtacapillary = 「緊貼微血管」的意思)。
怎麼啟動:三種刺激可以點燃它們[1]:
- 炎症介質(inflammation):肺炎、ARDS 時釋放的化學物質直接刺激這些神經末梢
- 吸入的化學刺激物或毒素(inhaled chemicals or toxins)
- 肺微血管壓力升高(increased pulmonary capillary pressures):這就是為什麼左心衰竭(left heart failure)的病人會喘——肺靜脈壓上升 → 肺微血管壓升高 → C 纖維被激活
神經路線:C 纖維 → 迷走神經(CN X) → 延髓孤束核(nucleus tractus solitarius, NTS)[1][2]。
產生的感覺與反射:激活後產生強烈的窒息感(air hunger)和反射性的快淺呼吸(rapid shallow breathing)[1]。這也是為什麼肺水腫病人的典型呼吸型態是又快又淺。
② 快適應型牽張受體(Rapidly Adapting Stretch Receptors, RARs)= Irritant Receptors
受體類型:有髓鞘的機械受體,位於氣道上皮層[1]。它們對刺激的反應很快但也很快就「適應」了(所以叫 rapidly adapting)。
怎麼啟動[1]:
- 吸入刺激物(inhaled irritants):冷空氣、煙霧、粉塵
- 支氣管收縮(bronchospasm):氣喘發作時支氣管壁的機械變形直接刺激這些受體
- 肺塌陷 / 肺不張(deflation of the lung / atelectasis):這解釋了為什麼大量胸腔積液(large pleural effusions)的病人會喘——積液壓迫 → 底部肺葉塌陷 → irritant receptors 被激活
神經路線:RARs → 迷走神經(CN X)有髓鞘 Aδ 纖維 → 延髓孤束核(NTS)[1][2]。
產生的感覺與反射:激活後產生「胸緊」(chest tightness)的感覺和咳嗽反射[1]。Murray 特別指出:氣喘病人描述的「胸口很緊」這個感覺,最可能就是來自 irritant receptors 被支氣管痙攣所刺激[1]。也會引發強烈的深吸氣衝動(urge to take a deep breath)。
③ 慢適應型牽張受體(Slowly Adapting Stretch Receptors, SARs)
受體類型:有髓鞘的機械受體,位於氣道平滑肌層[1][2]。
怎麼啟動:當肺充氣、潮氣量增大時,氣道被牽張 → SARs 被激活[1]。Guyton 描述的Hering-Breuer 膨脹反射就是由這些受體介導的[2]。
神經路線:SARs → 迷走神經(CN X) → 延髓孤束核(NTS) → 抑制吸氣神經元(inspiratory-off switch)[2]。
產生的效果:與其他受體不同,SARs 的激活反而減輕 air hunger[1]。原理是:肺膨脹的訊號告訴腦幹「吸氣任務有達成」,減少了 efferent-afferent dissociation(見 B1 節)。這也是為什麼深呼吸會讓人覺得舒服——SARs 回報「肺有好好膨脹」,讓大腦放心。
④ 壓力受體(Pressure Receptors / Vascular Receptors)
受體類型:機械感受器,分佈在肺血管系統和右心[1]。
怎麼啟動:肺動脈壓或右心壓力升高時被激活[1]。
神經路線:→ 迷走神經(CN X) → 延髓[1]。
臨床意義:這類受體解釋了為什麼原發性肺血管疾病(如肺動脈高壓 pulmonary hypertension)和左心衰竭(導致肺靜脈壓升高)的病人會有呼吸困難[1]。也有助於解釋肺栓塞(pulmonary emboli)時的 dyspnea——即使氣體交換還沒明顯惡化,血管壓力的變化就已經透過這些受體讓病人感到喘了。
⑤ 流量受體(Flow Receptors)
受體類型:本質上是溫度受體(temperature receptors),位於氣道黏膜[1]。
怎麼啟動:吸氣時空氣流過氣道 → 氣道黏膜被冷卻 → 溫度受體感知到溫度下降[1]。吸氣流速越快,冷卻效果越明顯,受體激活越強。
神經路線:上呼吸道的 flow receptors 主要經由三叉神經(CN V)傳入;下呼吸道的經由迷走神經(CN X)傳入[1]。
功能:它們提供吸氣流量的即時回饋,幫助大腦監測「呼吸肌有沒有真的在動」和「efferent-afferent matching 有沒有達成」[1]。
臨床應用:這就是為什麼電風扇吹臉或鼻導管氣流可以減輕 dyspnea[1]——涼涼的空氣流過鼻腔和臉部 → 刺激三叉神經區域的 flow receptors → 大腦收到「有空氣在流動」的訊號 → 減輕 air hunger。
⑥ 代謝受體(Metaboreceptors / Ergoreceptors)
受體類型:位於骨骼肌中的化學和機械感受器[1]。
怎麼啟動:當局部氧氣輸送不足(low oxygen delivery)時,肌肉產生乳酸和代謝廢物 → metaboreceptors 被激活[1]。
神經路線:→ 脊髓背根(dorsal root)→ 經由薄束核 / 楔束核(gracile/cuneate nuclei)上行 → 延髓呼吸中樞[1]。(注意:這是唯一不走迷走神經的呼吸感測器路線!)
臨床意義:Murray 特別強調[1]:metaboreceptors 在兩個情境下特別重要——運動到極限時(lactic acidosis)和心衰竭時(心輸出量不夠 → 肌肉缺氧)。這就是為什麼心衰病人不只是躺著喘,連走幾步路都喘——肌肉一動就缺氧 → metaboreceptors 拼命回報 → 呼吸驅動大幅增加。
呼吸相關受體總整理
以下表格整合 Guyton[2] 和 Murray[1] 的內容,把所有參與呼吸調控和 dyspnea 產生的受體列在一起:
| 受體名稱 | 位置 | 纖維類型 | 刺激 / 啟動條件 | 傳入神經 | 腦幹終點 | 產生的感覺或反射 | 引用 |
|---|---|---|---|---|---|---|---|
| 中樞化學受體 (Central chemoreceptors) |
延髓腹外側面 (ventrolateral medulla)、 retrotrapezoid nucleus |
中樞神經元 (不是周邊傳入) |
CO₂ 穿過血腦屏障 → 轉化為 H⁺ → 直接刺激 | 不適用 (就在腦幹內) |
化學敏感區 → DRG/VRG | Air hunger(吸不到氣);通氣量大幅增加 | [2] |
| 周邊化學受體 (Peripheral chemoreceptors) |
頸動脈體 (carotid body); 主動脈體 (aortic body) |
有髓鞘 傳入纖維 |
低氧(PaO₂ < 60 mmHg 才明顯);高 CO₂;低 pH | 頸動脈體 → 舌咽神經 CN IX; 主動脈體 → 迷走神經 CN X |
孤束核 (NTS) → DRG | Air hunger;通氣量增加 | [2] |
| 肺 C 纖維 (Pulmonary C fibers / J receptors) |
肺泡壁、 肺微血管旁 |
無髓鞘 C 纖維 |
炎症介質;吸入毒素;肺微血管壓升高(左心衰竭) | 迷走神經 CN X | 孤束核 (NTS) | 窒息感;反射性快淺呼吸 | [1] |
| 快適應型牽張受體 (RARs / Irritant receptors) |
氣道上皮層 | 有髓鞘 Aδ 纖維 |
吸入刺激物;支氣管收縮;肺塌陷 / 肺不張 | 迷走神經 CN X | 孤束核 (NTS) | 胸緊(chest tightness);咳嗽反射;深吸氣衝動 | [1] |
| 慢適應型牽張受體 (SARs) |
氣道平滑肌層 | 有髓鞘 傳入纖維 |
肺充氣、潮氣量增大 → 氣道被牽張 | 迷走神經 CN X | 孤束核 (NTS) → 抑制吸氣神經元 | Hering-Breuer 反射:終止吸氣;減輕 air hunger | [1][2] |
| 壓力受體 (Pulmonary vascular receptors) |
肺血管系統、 右心 |
機械感受器 | 肺動脈壓或右心壓力升高 | 迷走神經 CN X | 孤束核 (NTS) | 呼吸困難感(肺高壓、PE、左心衰竭時) | [1] |
| 流量受體 (Flow receptors) |
上下呼吸道黏膜、 鼻腔、臉部 |
溫度受體 | 吸氣氣流冷卻氣道黏膜 | 上呼吸道/臉部 → 三叉神經 CN V; 下呼吸道 → 迷走神經 CN X |
三叉神經核 / 孤束核 | 監測吸氣流量;減輕 air hunger(電扇吹臉的原理) | [1] |
| 代謝受體 (Metaboreceptors / Ergoreceptors) |
骨骼肌 | 無髓鞘 C 纖維 + 有髓鞘 Aδ |
局部缺氧 → 乳酸堆積、代謝廢物 | 脊髓背根 (不走迷走神經!) |
薄束核/楔束核 → 延髓呼吸中樞 | 費力感(effort);運動和心衰時呼吸驅動增加 | [1] |
從表格可以看出兩個規律[1][2]:
第一,肺內的受體(C 纖維、RARs、SARs、壓力受體、流量受體)幾乎都走迷走神經(CN X)送到延髓孤束核(NTS)。唯一的例外是臉部和鼻腔的流量受體走三叉神經(CN V)。所以迷走神經可以說是肺和腦幹之間的「高速公路」。
第二,大部分受體激活後都會增加呼吸困難感或呼吸驅動,只有一個例外——慢適應型牽張受體(SARs)反而會減輕 air hunger。這個特性在臨床上很有用:深呼吸、CPAP、甚至吸入 furosemide 氣霧劑刺激 SARs,都可能緩解 dyspnea[1]。
延伸討論:心臟缺血的「胸悶」— 一樣的感覺,不一樣的路線
學到這裡,聰明的你可能會問:缺血性心臟病(angina pectoris)也常讓病人描述「胸悶」——這跟氣喘病人因為 irritant receptors 引起的「胸緊」有什麼不同?是不是也是走迷走神經?
答案是:不是。兩者走的是完全不同的神經路線,但最終會在脊髓匯聚,所以感覺會很相似。以下用科學資料拆解。
心臟的感覺神經末梢
Rosen 在 2012 年的 review 中詳細整理了心臟痛覺的神經解剖[9]:心肌中的感覺神經末梢並非專一的痛覺受器,而是混合了有髓鞘的 Aδ 纖維和無髓鞘的 C 纖維,兩者都同時具有化學敏感性(chemosensitive)和機械敏感性(mechanosensitive)。
這些感覺末梢對什麼東西起反應?當心肌缺血時[9][10]:
- 腺苷(adenosine):缺血 → ATP/ADP 比值下降 → 腺苷大量累積 → 通過 A₁ 受體(為主)和 A₂ 受體激活交感傳入纖維。這是目前被認為最重要的心臟痛覺觸發物質。
- 緩激肽(bradykinin):化學和機械敏感末梢都對其起反應
- 其他:鉀離子(K⁺)、前列腺素(prostaglandins)、白三烯(leukotrienes)
- TRPV1 受體:回應氫離子(H⁺)、溫度變化 → 釋放 CGRP 和 substance P[9]
關鍵差異:走交感神經,不是迷走神經
這是最重要的一點。心臟缺血產生的疼痛訊號,主要走的是交感神經傳入路線(sympathetic afferents),而不是迷走神經[9][10]:
心肌感覺末梢 → 心臟交感神經叢(cardiac sympathetic plexus)→ 不換神經元直接通過交感神經鏈(sympathetic ganglion chain)→ 進入脊髓背角(dorsal horn)的 lamina I(主要)和 lamina V[10]
交感傳入纖維的細胞體位於 C8–T9 的背根神經節(dorsal root ganglia),尤其集中在 T2–T6[9]。訊號經由 Lissauer's tract 上行 → 主要走脊髓丘腦束(spinothalamic tract)→ 到達後側丘腦(posterior thalamus)。
迷走神經在心臟痛覺中扮演的角色相對次要[9][10]。Rosen 引用 Foreman 的研究指出:心臟的迷走傳入纖維主要連接到延髓的孤束核(NTS)→ 再到橋腦的臂旁核(parabrachial nucleus)→ 丘腦。Foreman 特別指出一個臨床相關的發現[9]:胸部和上臂的體感覺 convergence 傾向與交感傳入路線合併;而頸部和下巴的體感覺 convergence 傾向與迷走傳入路線合併。這就解釋了為什麼心絞痛有時候會放射到下巴和頸部(vagal pathway)。
為什麼心臟和呼吸道的「胸悶」會搞混?— Convergence
Leach & Fisher[10] 在他們的 review 中指出了關鍵的解剖事實:
氣管支氣管樹、肺臟、食道、和胃的傳入纖維,與心臟交感傳入纖維在同一個脊髓節段(upper thoracic segments)匯聚[10]。
在脊髓背角的 lamina I,這些來自心臟的內臟傳入神經元和來自胸壁的體感覺痛覺纖維(somatic nociceptive fibres)匯聚到同一群 lamina I 神經元上[10]。大腦無法區分訊號來自心臟還是來自胸壁或肺 → 都被解讀為「胸口不舒服」。
這就是為什麼很多病人——不管是心絞痛還是氣喘——都用類似的詞彙描述胸部不適:壓迫感、緊繃感、悶。Leach & Fisher 特別指出[10]:由於 visceral afferent 在脊髓中的匯聚本質是瀰漫性的(diffuse),大腦的感覺皮質無法精確地將訊號投射到「身體地圖」上,所以心絞痛的定位通常很差(用手掌或拳頭比,不是用手指指)。
兩條路線的比較總結
| 呼吸道的「胸緊」 (Chest tightness) |
心臟缺血的「胸悶」 (Anginal chest discomfort) |
|
|---|---|---|
| 觸發原因 | 支氣管收縮、吸入刺激物、肺塌陷[1] | 心肌缺血 → 腺苷、緩激肽、K⁺ 累積[9][10] |
| 受體 | Irritant receptors (RARs),有髓鞘 Aδ 纖維[1] | 混合 Aδ + C 纖維的 chemosensitive 和 mechanosensitive 末梢[9] |
| 主要傳入神經 | 迷走神經 CN X → 延髓 NTS[1] | 交感傳入神經 → 脊髓背角 T2-T6 lamina I/V[9][10] |
| 中樞投射 | NTS → 呼吸中樞 + 感覺皮質[1] | 脊髓丘腦束 → 後側丘腦 → 感覺皮質 + 邊緣系統[9] |
| 為什麼感覺相似 | 兩者的傳入纖維在上胸段脊髓(upper thoracic spinal cord)的 lamina I 匯聚到同一群神經元 → 大腦無法區分來源[10] | |
| 伴隨特徵 | 咳嗽、喘鳴、深吸氣衝動[1] | 放射到左臂/下巴(referred pain)、冒冷汗、噁心[10] |
| 定位精確度 | 與特定質感連結(如「胸緊」與支氣管痙攣)[1] | 瀰漫、定位差(用拳頭比而非手指指,即 Levine's sign)[10] |
呼吸道的「胸緊」走迷走神經 → 延髓;心臟缺血的「胸悶」走交感傳入神經 → 脊髓。兩者是完全不同的路線[1][9][10]。但因為肺和心臟的傳入纖維在上胸段脊髓 lamina I 匯聚到同一群神經元,大腦收到的訊號會混在一起[10],這就是為什麼病人常常說不清楚到底是「喘」還是「悶」——因為在脊髓層級,兩個訊號已經混合了。
臨床上,區分兩者要靠伴隨特徵而非僅靠「胸悶」這個詞本身——有沒有放射痛?有沒有喘鳴?跟運動還是跟姿勢有關?(這就是 Module C 會詳細討論的 History 五要素。)
A4 從機制到感覺的整合
Murray & Nadel's Figure 36.1[1] 是理解 dyspnea 知覺的關鍵圖。它顯示:所有感測器的訊號最終匯聚到大腦皮質的感覺區域,在那裡被整合成一個統一的「喘」的感覺。
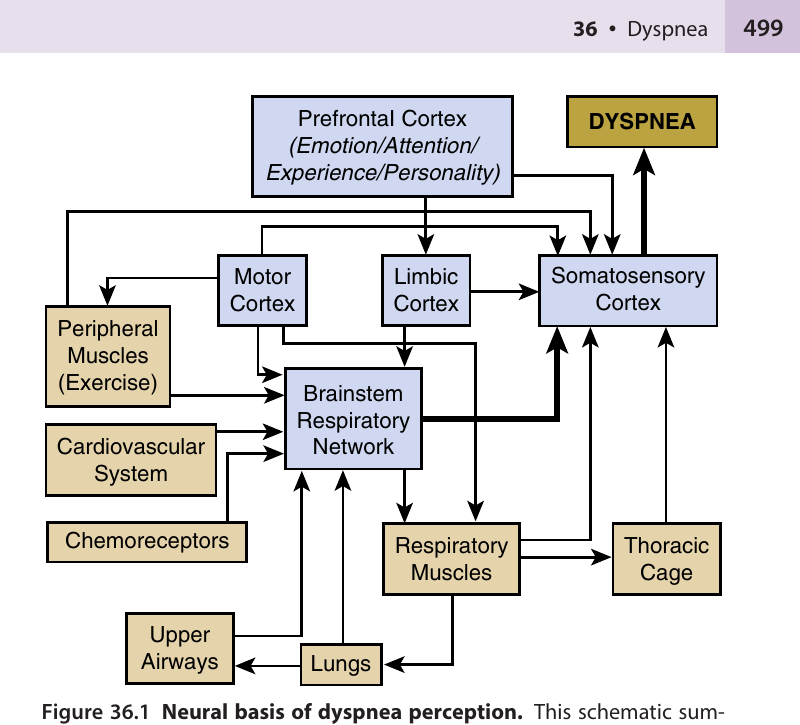
中文說明:Dyspnea 最終是一個「大腦的感覺」。不同偵探(化學受體、迷走神經末梢、肌肉受體)的報告通過不同的路徑送到皮質,在那裡融合成「喘」的體驗。注意圖中的前額皮質(Prefrontal Cortex)和邊緣系統(Limbic Cortex)——焦慮和情緒也能調整你對喘的感受。
Manning & Schwartzstein 在 1995 年的 NEJM 文章[3] 進一步釐清了不同感覺的神經路徑:
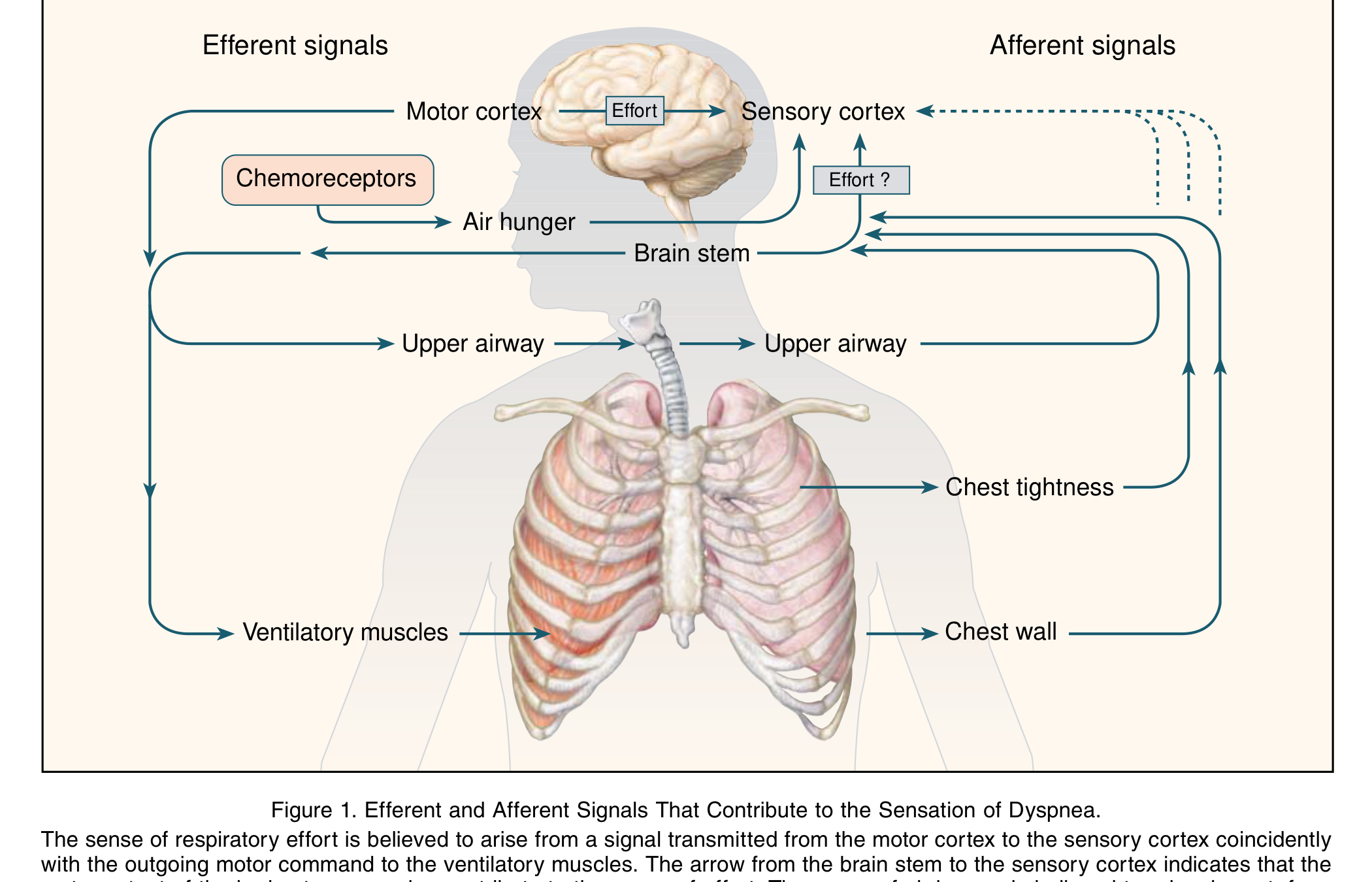
中文說明:Manning 的經典圖解:費力感(Effort)= 大腦運動皮質發出命令時的「感知複製」→ 你用力呼吸就感覺費力。吸不夠感(Air hunger)= 腦幹驅動很高但通氣不夠 → 一種渴求空氣的感覺。胸緊感(Tightness)= 氣道裡的迷走神經末梢被刺激 → 像被綁住。三種感覺、三條路徑、三種暗示。
呼吸控制 = 感測器 → 控制中樞 → 效應器[1,2]。
CO₂ 是最強的呼吸驅動者,通過血腦屏障直接作用於延髓[2]。
Dyspnea 有四種產生方式:血氣異常、感受器刺激、機械負荷、肌肉無力[1]。
不同機制產生不同「質感」的喘:air hunger、work/effort、chest tightness[1,3]。
B — 感覺與 PatternDyspnea 的質性描述與異常呼吸 Pattern
B1 五種質性描述
Murray & Nadel's Textbook 的 Table 36.1[1] 把 dyspnea 的「質性描述」、「對應的生理機制」和「常見疾病」整理成一個非常實用的對照表。Lansing 等人(2009)進一步用實驗證實了 air hunger 和 work/effort 是獨立的感覺[5]——你可以只有 air hunger 而不覺得費力,也可以只覺得費力但不覺得缺氧。
| 感覺描述(Quality) | 對應生理機制(Physiology) | 常見疾病(Disease States) |
|---|---|---|
| Air hunger 「吸不夠空氣」「缺氧感」「窒息感」 |
化學受體刺激呼吸控制中樞(via chemoreceptors, pulmonary receptors, vascular receptors) | Pneumonia, pulmonary edema, PE, COPD with acute gas exchange abnormalities, asthma, pleural effusion, toxic inhalations |
| Chest tightness 「胸口緊」「被綁住」 |
肺部 airway receptors 刺激 | Asthma, pulmonary edema with bronchospasm, toxic inhalations with bronchospasm |
| Cannot get a deep breath 「吸不飽」「吸不深」 |
呼吸控制中樞刺激 + dynamic hyperinflation | COPD, asthma |
| Increased work/effort 「呼吸很費力」「像拖重物」 |
呼吸系統機械負荷增加;神經肌肉衰弱 | COPD, asthma, obesity, kyphoscoliosis, Guillain-Barré, myasthenia gravis |
| Breathing more 「呼吸變多了」「喘氣」 |
通氣量增加 + 肌肉 metaboreceptors 刺激 | Exercise, cardiovascular deconditioning |
改編自 Murray & Nadel's Textbook, Table 36.1: Relationship Among Qualities of Dyspnea, Physiology, and Disease States[1]
為什麼 Air Hunger 特別痛苦?—— Efferent-Afferent Dissociation
在上表的五種感覺中,air hunger 是最令人痛苦的[1]。Schwartzstein & Adams 用一個概念來解釋為什麼:efferent-afferent dissociation——當大腦發出的呼吸命令(efferent)與實際產生的通氣量反饋(afferent)之間出現落差時,dyspnea 會被大幅放大[1]。
用白話說:大腦命令「多吸一點!」,但身體做不到(因為氣道阻塞、肺變硬、或肌肉無力)。大腦感覺到自己的命令沒有被執行 → 產生極度不適的 air hunger[1]。
臨床上最常見的場景[1]:
- COPD 的 dynamic hyperinflation:運動時呼氣不完全 → 肺過度膨脹 → 膈肌力學劣勢 → 大腦要求更多通氣但做不到 → 強烈 air hunger
- 心衰竭:呼吸肌供血不足、肺順應性降低 → 同樣的驅動產生更少的通氣 → air hunger
- Breath-holding是極端例子——你故意停止呼吸,而大腦驅動持續上升但沒有任何通氣反饋 → 最純粹的 air hunger
Schwartzstein & Adams 進一步指出[1]:如果能增加 afferent feedback(如 volume-related feedback from stretch receptors),就能縮小這個落差、減輕 air hunger。這就是為什麼 COPD 患者使用吸入 furosemide(激活 slowly adapting stretch receptors)或臉部吹涼風(激活三叉神經面部感受器)可能緩解喘感。
B2 感覺的情感維度
Schwartzstein & Adams[1] 強調:air hunger 比 work/effort 會引發更強烈的情感反應。當 air hunger 非常嚴重時,病人會用「窒息」(suffocating)來形容——這個詞在輕度 dyspnea 時幾乎不會出現。
Murray & Nadel's Textbook 提到[1]:
- Dyspnea 在出乎意料時更令人不安(unexpected dyspnea is worse than expected)
- 病人如果覺得這個喘是危險的,感受會更強烈
- 焦慮會獨立於呼吸驅動地加重 dyspnea 感覺
- 在過度換氣症候群(hyperventilation syndrome)中,焦慮本身就能驅動強烈的呼吸困難,即使沒有任何生理刺激
B3 五種異常呼吸 Pattern
除了「聽病人怎麼說」,醫生還可以「看病人怎麼呼吸」。Murray & Nadel's Table 36.2[1] 整理了理學檢查所見與病理的對應關係。以下是最重要的幾種異常呼吸 Pattern:
| 呼吸 Pattern | 特徵 | 生理機制 | 常見原因 |
|---|---|---|---|
| Kussmaul 呼吸 | 深而快,有規律(deep rapid breathing with a lower VD/VT ratio)[1] | 代謝性酸中毒刺激化學受體 → 大量增加肺泡通氣以排出 CO₂ 代償酸血症 | DKA, severe lactic acidosis, ingestions leading to anion gap acidosis[1] |
| Cheyne-Stokes 呼吸 | 週期性:呼吸漸進加深(crescendo)→ 漸進減淺(decrescendo)→ 短暫無呼吸(apnea)→ 重複 | 中樞化學反射敏感性↑ + 肺循環延遲(prolonged circulation time)→ 呼吸反饋迴路不穩定[2,6] | Advanced HFrEF(最常見,30-50% 患者), brainstem stroke[6,7] |
| Biot's 呼吸 | 不規則呼吸:幾次正常呼吸 → 突然停止 → 不可預測地重新開始 | 腦幹呼吸中樞嚴重受損,失去節律生成能力[2] | Brainstem stroke, 顱內高壓, severe head trauma |
| Paradoxical 呼吸 | 吸氣時腹部內陷,呼氣時腹部外凸(正常相反) | 膈肌麻痺或極度衰弱 → 吸氣時胸腔負壓將無力的膈肌往上拉[1] | Diaphragm paralysis, spinal cord injury, severe neuromuscular disease (GBS, MG)[1] |
| Tachypnea + 輔助呼吸肌 | 呼吸快,使用胸鎖乳突肌、斜角肌等輔助呼吸肌 | 呼吸驅動增加 + 呼吸系統機械負荷增加 → 需要更多肌力代償[1] | Pneumonia, PE, COPD exacerbation, asthma, pleural effusion[1] |
Cheyne-Stokes 呼吸:心臟科最重要的異常 Pattern
Guyton[2] 用 Figure 42.12 解釋了 Cheyne-Stokes 呼吸的機制:當血液從肺到腦的傳輸時間過長(如心輸出量低的心衰竭),化學受體的反饋出現延遲。大腦接收到的 CO₂ 資訊已經過時了——結果就像一個「延遲的恆溫器」,反應過度然後又過度修正,形成週期性的oscillation。
Braunwald's Heart Disease[7] 指出:Cheyne-Stokes respiration(也稱為 periodic or cyclic respiration)在晚期 HF 中很常見,通常與低心輸出量和睡眠障礙性呼吸相關。CSR 的存在是預後不良的獨立指標。
Yumino & Bradley[6] 詳細闡述了 HF 中 CSR 的五個驅動因素:(1) 化學反射敏感性升高,(2) 肺循環傳導延遲使 loop gain 升高,(3) 無呼吸期間低氧進一步刺激化學受體,(4) 交感神經激活維持高基礎驅動,(5) 過度通氣使 PaCO₂ 低於 apneic threshold 觸發無呼吸。
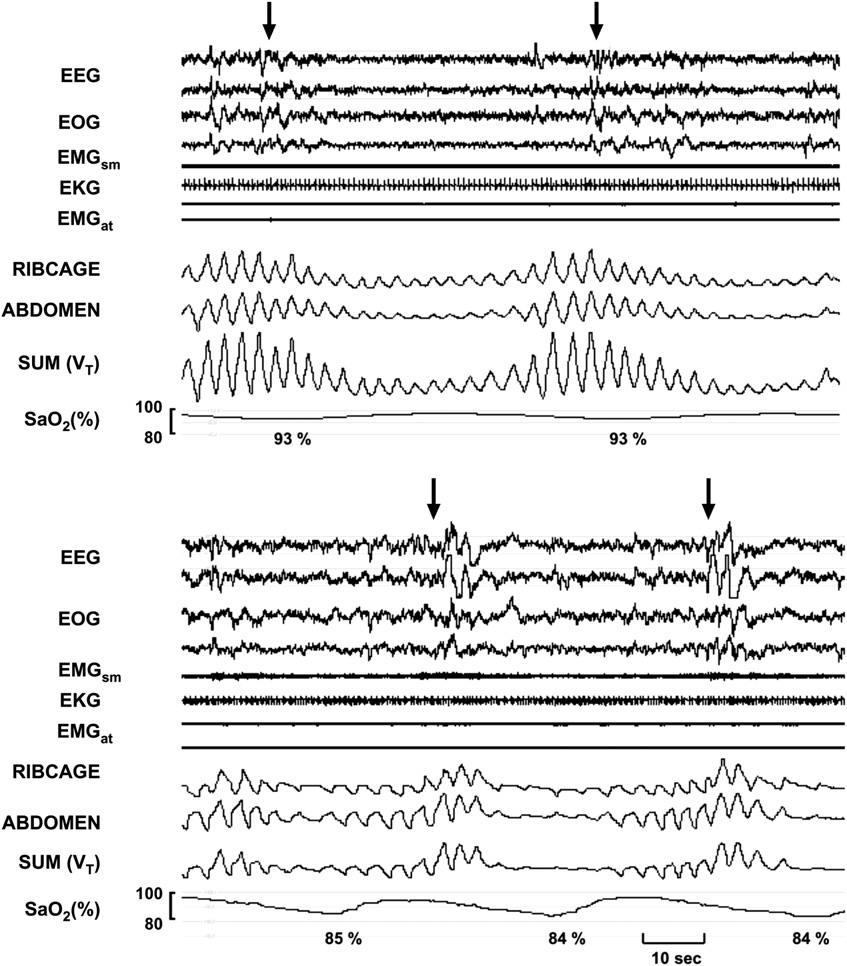
中文說明:這是 CSR 的睡眠多導圖(PSG)記錄。上方面板顯示心衰患者的中樞性低通氣。注意潮氣量的「漸強-漸弱」週期性波動——這就是 CSR 的典型特徵。
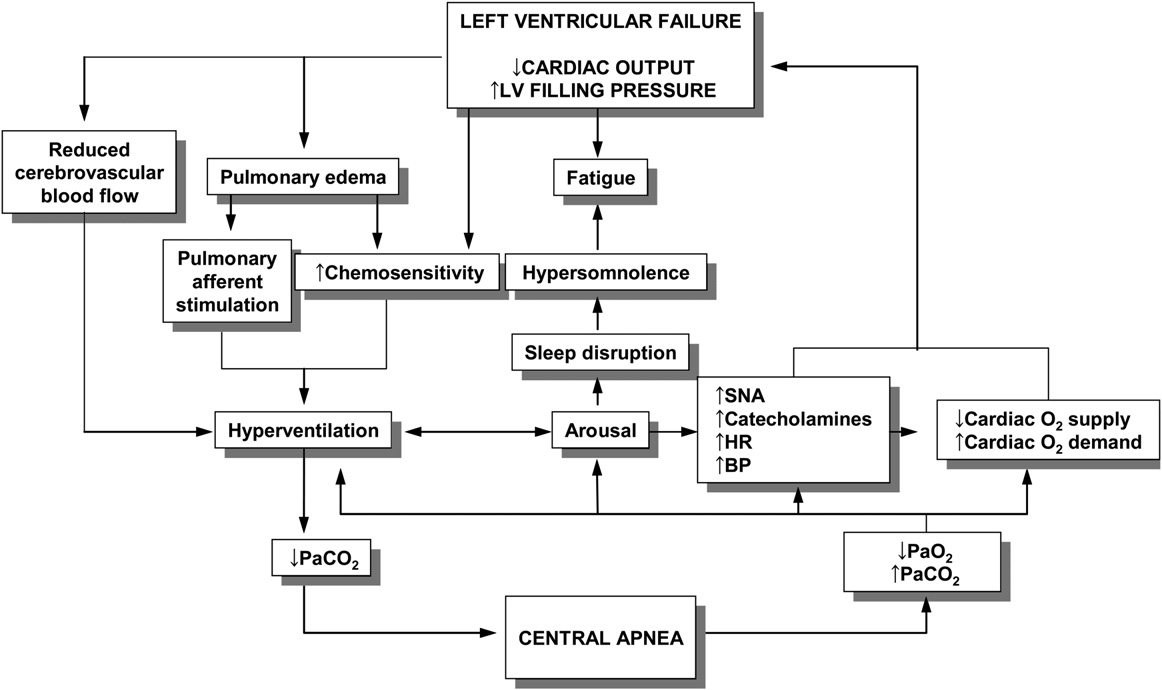
中文說明:HF 中 CSR 的病理生理示意圖,五個因素互相強化:化學受體過度敏感 → 通氣過度 → CO₂ 降太低 → 觸發無呼吸 → 低氧又刺激化學受體 → 惡性循環。肺循環延遲(心輸出量低)使這個迴路更不穩定。
B4 姿勢相關 Pattern
Murray & Nadel's Textbook[1] 指出,問診時 dyspnea 的姿勢相關性(positional nature)是五大資訊之一。Braunwald's Heart Disease[7] 進一步描述了各種姿勢相關症狀在 HF 中的意義:
| 姿勢 Pattern | 定義 | 機制 | 最常見原因 |
|---|---|---|---|
| Orthopnea 端坐呼吸 |
平躺時喘加重,需抬高頭或坐起 | 平臥 → 靜脈回流↑ → 肺靜脈壓↑ → 肺充血 → 肺順應性↓ + 肺 C 纖維刺激[7] | Left heart failure, mitral valve disease[7] |
| PND 夜間陣發性呼吸困難 |
睡眠中突然驚醒喘不過氣 | 平臥數小時 → 肺充血逐漸加重 → 突破閾值 → 化學受體被激活 → 驚醒[7] | Braunwald 稱 PND 是「HF 最可靠的指標之一」(one of the most highly reliable indicators of HF)[7] |
| Trepopnea | 只有側臥某一邊時才會喘 | Braunwald[7]: dyspnea while lying on the left side, 可能與肺血管壓力分布不對稱有關 | Large pleural effusion, HF |
| Platypnea | 站立或坐起時喘,平躺反而好 | 站立 → 右至左分流增加 → 低血氧[1] | Hepatopulmonary syndrome, PFO with R-to-L shunt[1] |
| Bendopnea | 前彎(如繫鞋帶)時呼吸困難 | 前彎 → 腹壓↑ → 膈肌上推 → 心臟充盈壓↑ → 肺充血[1] | HFpEF, HFrEF, restrictive pericardial disease[1] |
C — Bench to Bedside問診與觀察的臨床應用
C1 問診五要素
Murray & Nadel's Textbook[1] 明確指出:評估呼吸困難的病人時,病史應該聚焦在五種資訊:
- 語言(Language):病人怎麼描述他的喘?
- 時間(Timing):急性、間歇性、還是慢性?
- 姿勢(Position):跟姿勢有關嗎?
- 伴隨症狀(Associated symptoms):有沒有其他線索?
- 強度(Intensity):多嚴重?對日常生活影響多大?
1. 語言(Language)—— 最重要的第一步
Schwartzstein & Adams 寫道[1]:就像醫生會問胸痛的「質感」(sharp, dull, burning, aching),同樣的方法也適用於呼吸困難。最好先問病人:「你的呼吸不舒服到底是什麼感覺?」如果病人不知道怎麼形容,可以提供一些選項讓他選最接近的三個[1]。
根據 Murray Table 36.1[1],病人使用的描述詞與疾病的對應關係如下:
- 「吸不到空氣 / 缺氧 / 窒息感」(Air hunger)→ 化學受體刺激 → 想到 pneumonia、pulmonary edema、acute gas exchange abnormalities
- 「胸口很緊 / 被綁住」(Chest tightness)→ 氣道 receptors 刺激 → 想到 asthma、bronchospasm
- 「吸不飽 / 吸不深」(Cannot get a deep breath)→ dynamic hyperinflation → 想到 COPD、asthma
- 「呼吸很費力 / 像拖重物」(Increased work/effort)→ 機械負荷↑ 或肌肉無力 → 想到 COPD、obesity、kyphoscoliosis、neuromuscular disease
- 「呼吸變多了 / 一直在喘」(Breathing more)→ 通氣量增加 → 想到 exercise、deconditioning
2. 時間(Timing)
Schwartzstein & Adams[1] 的歸納:
- 急性 dyspnea:asthma, pulmonary edema, pneumonia, PE, 以及與↑ airway resistance / ↓ pulmonary compliance 相關的疾病
- 間歇性 dyspnea:最常見的是運動時喘。COPD、interstitial lung disease、pulmonary vascular disease、chronic HF、supply-demand ischemic heart disease 都可以間歇性發作。此外要詢問:運動以外有沒有其他觸發因素(如環境暴露)?
- 慢性持續性 dyspnea(靜息時):代表嚴重的末期心肺疾病——severe COPD 或 severe HF。也要考慮 progressive neuromuscular disease(如 ALS)[1]
3. 姿勢(Position)
見 Module B5 的姿勢相關 Pattern 表格[1,7]。重點:Orthopnea 和 PND 對左心衰竭的診斷價值極高。Braunwald 稱 PND 是 HF 最可靠的指標之一[7]。
4. 伴隨症狀(Associated Symptoms)
Schwartzstein & Adams[1] 指出,因為 dyspnea 可以來自很多疾病,伴隨症狀是縮小鑑別診斷的關鍵:
- 下肢水腫 + 夜間驚醒喘 → likely heart failure[1]
- 交替性畏寒發燒 + 咳嗽 → likely respiratory infection[1]
- 瀰漫性肌肉無力 → may be associated with respiratory muscle dysfunction[1]
- 胃酸逆流 + 燒灼感 → clue to recurrent aspiration[1]
- 皮膚變化:erythema nodosum(sarcoidosis)、Raynaud's phenomenon(scleroderma with ILD)[1]
5. 強度(Intensity)
Schwartzstein & Adams 提醒[1]:不要把理學檢查看到的「呼吸窘迫徵象」跟病人自己感受的 dyspnea 混為一談。醫生和護理師常常低估病人的喘的程度。而且,病人會改變生活方式來避免喘——如果爬樓梯會喘,他就搬到一樓;如果買菜太喘,就叫家人代勞。所以你可能看不出來他的功能已經嚴重下降[1]。
C2 理學檢查怎麼看
Murray & Nadel's Table 36.2[1] 整理了理學檢查所見與病理生理的對應。Braunwald's Heart Disease Table 56.4[7] 進一步提供了各項 H&P findings 對 HF 診斷的 sensitivity 和 specificity。
| 理學檢查所見 | 生理機制 | 常見疾病 |
|---|---|---|
| Tachypnea + 輔助呼吸肌 (SCM, scalene) |
呼吸驅動↑(via chemoreceptors, pulmonary receptors, vascular receptors)[1] | Pneumonia, PE, COPD exacerbation, asthma, pleural effusion, toxic inhalations[1] |
| Pulsus paradoxus >10 mmHg + wheezes |
Pulmonary receptors 刺激 + 氣道阻力增加[1] | Asthma, pulmonary edema with bronchospasm[1] |
| Paradoxical breathing (吸氣時腹部內陷) |
膈肌麻痺或極度衰弱[1] | Diaphragm paralysis, GBS, MG, spinal cord injury[1] |
| Expiratory abdominal rounding | 呼氣時腹部用力向外推,試圖產生 intrinsic PEEP[1] | Pulmonary edema(急性)[1] |
| Kussmaul 呼吸 (深、快、規律) |
代謝性酸中毒 → 增加肺泡通氣代償[1] | DKA, severe lactic acidosis, anion gap acidosis[1] |
| Crackles/rales | 肺順應性降低[1] | ILD, pneumonia, pulmonary edema[1] |
| Wheezes | 氣道阻力增加,turbulent flow[1] | Asthma, COPD, bronchitis[1] |
| JVP↑ + 下肢水腫 + S3 | 右心充盈壓↑,心輸出量↓[7] | Heart failure(S3: sensitivity 62%, specificity 32% per Braunwald Table 56.4)[7] |
C3 整合速查表
以下表格整合了 Murray Table 36.1[1](感覺→機制→疾病)、Table 36.2[1](理學檢查→機制→疾病)和 Braunwald's[7](HF 的症狀與徵象),形成一個 Bench-to-Bedside 的整合速查表:
| 病人說… | 你看到… | Bench 機制 | 首先想到… |
|---|---|---|---|
| 「吸不到空氣」 Air hunger |
Kussmaul 呼吸(深、快) | 代謝性酸中毒 → 化學受體刺激 → 中樞驅動↑[1,2] | DKA, lactic acidosis, uremia, toxic ingestion[1] |
| 「吸不到空氣」 Air hunger |
Cheyne-Stokes(週期性)+ JVP↑ + edema | HF → 循環延遲 + 化學反射敏感性↑ → 反饋迴路不穩定[2,6,7] | Advanced HFrEF, brainstem stroke[6,7] |
| 「呼吸很費力」 Work/effort |
Tachypnea + accessory muscle use + wheezes | 機械負荷↑ → 呼吸肌感知複製↑[1,3] | COPD, asthma, obesity, kyphoscoliosis[1] |
| 「呼吸很費力」 Work/effort |
Paradoxical breathing(吸氣腹部內陷) | 膈肌衰弱 → efferent-afferent dissociation[1] | Diaphragm paralysis, GBS, MG[1] |
| 「胸口很緊」 Tightness |
Wheezes ± tachypnea | Airway irritant receptors / C fibers 刺激[1,3] | Asthma, bronchospasm[1] |
| 「平躺就喘」 Orthopnea |
Crackles + JVP↑ + S3 | 平臥→肺充血→肺 C 纖維刺激 + 肺順應性↓[7] | Left HF, mitral valve disease[7] |
| 「睡到一半喘醒」 PND |
Tachypnea + crackles(發作時) | 數小時平臥→肺充血逐漸加重→突破閾值→驚醒[7] | HF(Braunwald 稱 PND 是 HF 最可靠指標之一[7]) |
| 「站起來才喘」 Platypnea |
Orthodeoxia(站立 SpO₂↓) | 站立→R-to-L shunt↑→低血氧[1] | Hepatopulmonary syndrome, PFO[1] |
| 不規則呼吸 意識改變 |
Biot's 呼吸(不規則停頓) | 腦幹呼吸中樞嚴重受損[2] | Brainstem stroke, ↑ICP, severe head trauma[2] |
Schwartzstein & Adams 的建議:與其問「哪個器官有問題」,不如先想「呼吸系統的哪個環節出了問題」——是 controller?sensor?effector?還是 gas exchanger?然後再根據感覺質性、呼吸 Pattern、和伴隨線索縮小鑑別診斷。
References
- [1] Schwartzstein RM, Adams L. Dyspnea. In: Broaddus VC, Ernst JD, King TE Jr, et al., eds. Murray & Nadel's Textbook of Respiratory Medicine. 7th ed. Philadelphia: Elsevier; 2022: Chapter 36, pp. 497–507.
- [2] Hall JE, Hall ME. Regulation of Respiration. In: Guyton and Hall Textbook of Medical Physiology. 15th ed. Philadelphia: Elsevier; 2026: Chapter 42, pp. 541–550.
- [3] Manning HL, Schwartzstein RM. Pathophysiology of dyspnea. N Engl J Med. 1995;333(23):1547–1553.
- [4] Weinberger SE, Cockrill BA, Mandel J. Control of Ventilation. In: Principles of Pulmonary Medicine. 7th ed. Philadelphia: Elsevier; 2019: Chapter 23.
- [5] Lansing RW, Gracely RH, Banzett RB. The multiple dimensions of dyspnea: review and hypotheses. Respir Physiol Neurobiol. 2009;167(1):53–60.
- [6] Yumino D, Bradley TD. Central sleep apnea and Cheyne-Stokes respiration. Proc Am Thorac Soc. 2008;5(2):226–236.
- [7] Januzzi JL, Mann DL. Clinical assessment of heart failure. In: Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine. 12th ed. Philadelphia: Elsevier; 2026: Chapter 56.
- [8] Parshall MB, Schwartzstein RM, Adams L, et al. An official American Thoracic Society statement: update on the mechanisms, assessment, and management of dyspnea. Am J Respir Crit Care Med. 2012;185(4):435–452.
- [9] 🟢 Rosen SD. From Heart to Brain: The Genesis and Processing of Cardiac Pain. Can J Cardiol. 2012;28(2 Suppl):S7–S19.
- [10] 🟢 Leach A, Fisher M. Myocardial ischaemia and cardiac pain – a mysterious relationship. Br J Pain. 2013;7(1):23–30. PMID: 26516494.